Article précédent

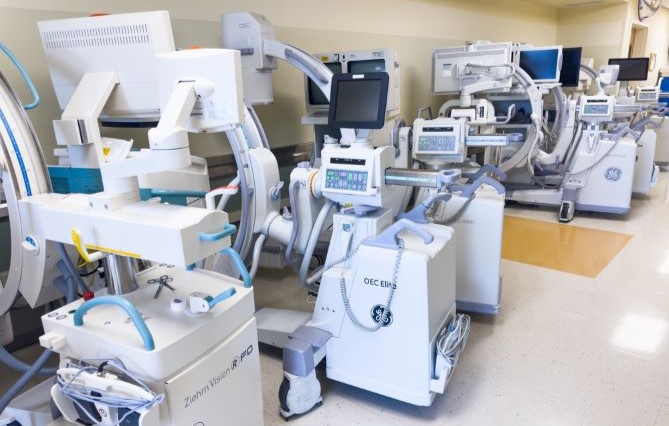
Le règlement européen relatif aux dispositifs médicaux [règlement (UE) 2017/745], entré en vigueur le 26 mai 2021, impose des obligations aux fabricants comme aux différents acteurs de la chaîne de distribution pour renforcer la qualité et la sécurité des produits au sein de l’Union européenne. En 2023, la période de transition pour l’adaptation aux nouvelles règles a été prolongée. Où en sommes-nous aujourd’hui alors que mai 2024 constitue une étape clés du processus ? Rappel et point de situation.
En France, selon les estimations (1), entre 800 000 et 2 millions de dispositifs médicaux (DM) sont actuellement commercialisés. Indispensables au diagnostic, au traitement et à la surveillance de nombreuses pathologies, ils sont d’une très grande hétérogénéité : bistouris électriques, appareils IRM, implants, pansements, seringues, fauteuils roulants… Ils sont toutefois soumis à une règlementation unique au sein de l’UE : un règlement européen [règlement (UE) 2017/745] entré en application le 26 mai 2021(2), adopté en remplacement de divers directives préexistantes (3). Le texte, qui couvre la conception, l’évaluation, la mise sur le marché et la surveillance post-commercialisation de ces produits de santé en Europe, a notamment pour ambition de renforcer leur qualité et leur sécurité.
Le texte s’applique aux futurs dispositifs comme à ceux déjà mis sur le marché. Les fabricants ont, par exemple, pour obligation de préciser et mettre à jour leurs étiquetages et notices d’utilisation, mais aussi de générer un identifiant unique (IUD) pour chacun de leurs produits afin d’en améliorer la traçabilité et de mieux lutter contre le risque de contrefaçons. Ils doivent également, dans certains cas, fournir de nouvelles données cliniques pour confirmer l’efficacité et la performance de leurs produits et dans tous les cas, mettre à jour leurs documentations techniques au regard des exigences revues du règlement. Une partie de ces données ont vocation à être implémentées dans une base de données européenne baptisée « Eudamed », toujours en cours de déploiement à ce jour. En partie publique, elle permettra, à terme, aux patients comme aux professionnels de santé d’avoir accès à des informations sur les dispositifs médicaux commercialisés en Europe, de connaître les éventuels incidents déclarés ainsi que l’avancée des investigations cliniques (lire encadré).
Les mandataires, les importateurs et les distributeurs de DM sont eux aussi visés par le texte. « Lorsqu’un distributeur considère ou a des raisons de croire qu’un dispositif n’est pas conforme aux exigences du présent règlement, il ne met le dispositif à disposition sur le marché
Débloquez immédiatement cet article pour 1 €, ou abonnez-vous pour accéder à l'ensemble de nos contenus.
THÉMATIQUES ASSOCIÉES
Infos locales, analyses et enquêtes : restez informé(e) sans limite.
Recevez gratuitement un concentré d’actualité chaque semaine.
0 Commentaire
Laisser un commentaire
Votre adresse e-mail ne sera pas publiée. Les champs obligatoires sont indiqués avec *